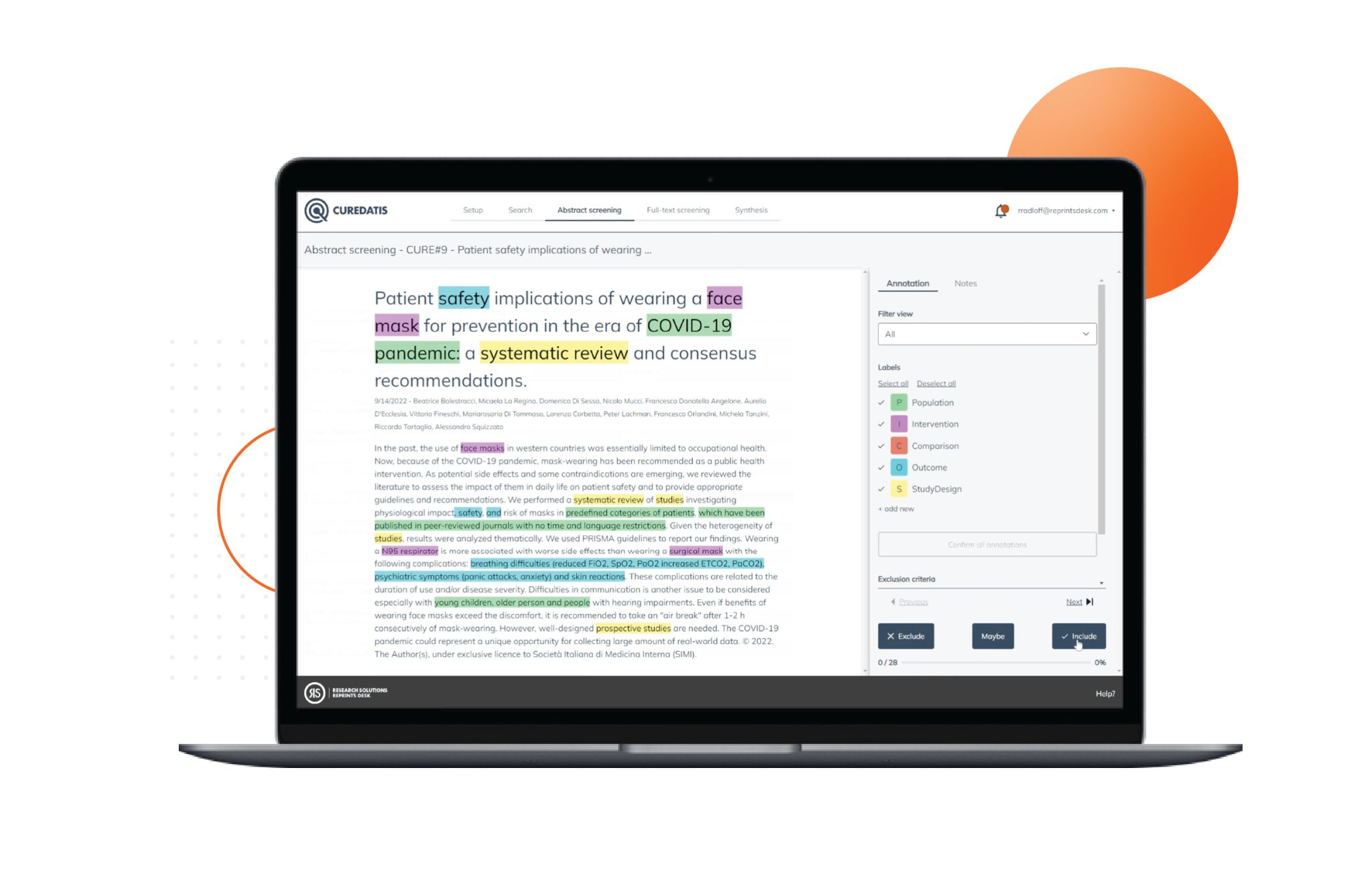
Klinische Studien – dafür steht das C3 in unserem 4C-Konzept. Zu unserem C3 gehört auch die klinische Bewertung, ein zentraler Prozess für Medizinproduktehersteller und solche, die es werden wollen. Wir haben mit Robert Radloff, Direktor für Produktentwicklung bei Research Solutions, über die Bedeutung des Prozesses, wie dieser intelligent umgesetzt werden kann und was das alles mit Wissensmanagement zu tun hat gesprochen.
Der Bericht zur klinischen Bewertung (Clinical Evaluation Report, CER) eines Medizinprodukts ist eines der wichtigsten regulatorischen Dokumente – warum?
Robert Radloff: Die klinische Bewertung ist ein systematischer Prozess, der für die Hersteller von Medizinprodukten für das Inverkehrbringen eines Produkts auf dem europäischen Markt obligatorisch ist. Zweck der Bewertung ist die objektive Dokumentation, dass das Produkt sicher und leistungsfähig ist, und der Nachweis der Übereinstimmung mit der EU-Medizinprodukteverordnung (MDR).
Warum ist eine systematische, gut geplante und dokumentierte initiale Literaturrecherche und -bewertung so wichtig?
RR: Der CER beinhaltet Beiträge von einer Vielzahl interner Akteure und die Integration zahlreicher Dokumente aus verschiedenen Abteilungen. Der Bericht ist auch eng mit anderen regulatorischen Prozessen verknüpft, wie dem Risikomanagement, der Überwachung nach dem Inverkehrbringen (Post-Market Surveillance, PMS) und der klinischen Nachbeobachtung nach dem Inverkehrbringen des Produkts (Post-Market Clinical Follow-up, PMCF). Die verschiedenen Informationsströme und Verbindungen machen einen systematischen und gut dokumentierten Prozess zu einem entscheidenden Faktor für den Erfolg eines CERs.
Bei einem so komplexen Prozess wie der klinischen Bewertung , wo fängt man am besten an?
RR: Als erster Schritt ist ein Plan zur klinischen Bewertung erforderlich. Darin werden die Methodik und der Umfang des klinischen Bewertungsprozesses beschrieben, einschließlich der Methodik für eine systematische Literatursuche. Aus klinischer Sicht sollte dieses Dokument einen grundlegenden Überblick über Folgendes geben:
- Klinischer Hintergrund und aktueller Wissensstand für die vorgesehene Verwendung des Produkts einschließlich Stand der Technik;
- Geräte- und äquivalente gerätespezifische klinische Daten aus der wissenschaftlichen Literatur und unveröffentlichte Herstellerdaten; und
- Analyse der klinischen Daten zu Sicherheit, Risiko, Leistung und Nutzen des Produkts.
Die klinische Bewertung und die systematische Literaturrecherche sollten von Anfang an als ein zentraler Prozess des Wissensmanagements verstanden werden, richtig?
RR: YJa, absolut! Der CER sollte nämlich nicht nur als regulatorische Anforderung, sondern auch als eine gerätespezifische Informationsbasis betrachtet werden. In einem idealen Szenario halten die verschiedenen Akteure innerhalb des Unternehmens, einschließlich F&E, Produktmanagement, Clinical Affairs und Vertrieb, diese Informationen auf dem neuesten Stand, sodass sie funktionsübergreifend innerhalb der Organisation verfügbar sind. Potenzielle Anwendungsfälle für eine strukturierte Literatur-Review sind neben der klinischen Bewertung:
- Evaluierung von Forschungsmethoden
- Wissenschaftliches Marketing
- Wettbewerbsbeobachtung
- Patentüberwachung
Gibt es Normen, Standards und andere Hilfsmittel, die du jungen Startups mit auf den Weg geben würdest?
Eines ist klar: Die klinische Bewertung ist ein zentraler Prozess für Medizinproduktehersteller. Wenn dieses Arbeitspaket frühzeitig, systematisch und mit Hilfe von intelligenten Tools angegangen wird, spart man wichtige Ressourcen wie Zeit und Geld. Gleichzeitig baut man damit eine interne Wissensbasis auf, die über die klinische Bewertung hinaus von Nutzen ist.
Roberts Literaturtipps:
Klinische Bewertung und systematische Reviews:
- MDR (EU) 2017/745 und MEDDEV 2.7/1 rev 4
- MDCG-Leitlinie 2020-06
- Cochrane Handbook of Systematic Reviews
Wissensmanagement:
- ISO 30401 – Wissensmanagement
- BIOPRO Leitfaden “Wissensmanagement“
Interview aus dem Englischen übersetzt.
Robert Radloff
Robert hat mehr als ein Jahrzehnt Erfahrung in der pharmazeutischen und medizintechnischen Industrie. Er hat zu mehreren Veröffentlichungen im Bereich der klinischen und regulatorischen Forschung beigetragen und ist ein starker Befürworter des Open-Innovation-Ansatzes.